|
Mit einer Inzidenz von 30- 35 pro 100.000 Einwohner ist das kolorektale Karzinom (KRK) eine der häufigsten malignen Erkrankungen der westlichen Welt. Insgesamt zeigen sich in der Inzidenz großeUnterschiede mit niedrigen Karzinomraten in Entwicklungsländern (z.B. 3,4 Karzinomfälle pro 100.000 Menschen in Nigeria) und hohen Inzidenzraten in Industrieländern (z.B. 35,8 Fälle pro 100.000 Menschen in Connecticut). Innerhalb der europäischen Union zeigen
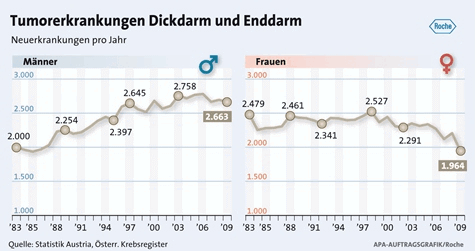
epidemiologische Untersuchungen ein signifikant höheres Auftreten des KRK in nördlichen und westlichen als in südlichen Ländern. Das KRK ist für etwa 15 % aller Krebstodesfälle verantwortlich. Männer sind etwas häufiger betroffen als Frauen. Durchschnittlich 5000 Neuerkrankungen pro Jahr in Österreich, diese Zahl entspricht 14% aller Krebsneuerkrankungen, machen das KRK zu einer beachtlichen Krankheitsentität. In Österreich liegt das KRK bei Männern nach dem Prostata- und Lungenkarzinom an dritter und bei Frauen nach dem Mammakarzinom sogar an zweiter Stelle. Das Risiko, an KRK zu erkranken, ist bis zum 45. beziehungsweise 50. Lebensjahr niedrig (nur 7% der KRK treten vor dem 50. Lebensjahr auf) und steigt etwa ab dem 50. Lebensjahr stark an. Der Altersgipfel liegt in Österreich bei Männern zwischen dem 65. und 74. und bei Frauen im 75. Lebensjahr und darüber. Das lebenslange Risiko an einem KRK zu erkranken beträgt 6%10 . 2005 erkrankten 4995 Patienten an einem KRK, wobei Männer mit 2.711 Fällen stärker betroffen waren als Frauen (2284 Neuerkrankte). Bei einer relativ stabilen Gesamtzahl von 4800 bis 5000 Neuerkrankungen pro Jahr, zeigt sich eine unterschiedliche Entwicklung der beiden Geschlechter. Während 1985 in absoluten Zahlen mehr Frauen als Männer an Darmkrebs
erkrankten, waren es 1995 in etwa gleich viele, und bis 2005 kehrte sich das Verhältnis (beginnend im Jahr 1996) um. Das Lebenszeitrisiko an kolorektalem Krebs zu versterben liegt in der Allgemeinbevölkerung bei etwa 3%. Die Mortalität steigt 10 Jahre nach dem Inzidenzanstieg an. Der durchschnittliche an Dickdarmkrebs versterbende Patient verliert durchschnittlich 13 Jahre seines Lebens. In Österreich sind die altersstandardisierten Inzidenzratendes kolorektalen Karzinoms mit 34,7 in Tirol und Niederösterreich am höchsten, während sie in Vorarlberg und Wien mit 22,1 und 29,1 am niedrigsten ist. Die Sterblichkeit an Darmkrebs ist in Tirol und in Kärnten am niedrigsten und in Burgenland, Niederösterreich und Wien am höchsten, Statistik Austria 2005/2007.
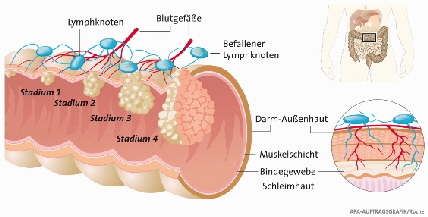
Das kolorektale Karzinom macht 95% der bösartigen Darmtumore aus. Zu ca. 95% bildet sich das Kolonkarzinom aus den Drüsen der Darmschleimhaut, es handelt sich also fast ausschließlich um Adenokarzinome. 80% davon sind differenzierte Adenokarzinome, 10% muzinöse Adenokarzinome und weitere 10% stellen undifferenzierte, anaplastische (hochmaligne) Karzinome dar. Die verbleibenden 5%, welche allesamt eine sehr schlechte Prognose haben, setzen sich aus Plattenepithelkarzinom des Analkanals, Leiomyosarkom, malignes Karzinoid, gastrointestinaler Stromatumor sowie Kaposi-Sarkom des Verdauungstrakts bei AIDS zusammen. Etwa 90% aller jährlich neu auftretenden kolorektalen Karzinome dürften sporadischer Natur sein. Sie entstehen über die Entwicklung aus adenomatösen Polypen und diese wiederum aus klinisch fast immer stummen Polypen. Dickdarmpolypen lassen sich unterteilen in hyperplastische, nicht- neoplastische und neoplastische Formen. Sie können ein gestieltes, sessiles oder flaches Wachstum aufweisen. Je breitbasiger beziehungsweise flacher sich ein Polyp makroskopisch darstellt, desto höher ist das Entartungsrisiko. Adenome sind epitheliale Formen von neoplastischen Polypen und machen etwa 80% aller Polypen aus. Diese haben als einzige Form der Polypen das Potential zur malignen Entartung, sind also als Präkanzerosen zu bezeichnen. Die Entartung läuft vom Adenom über die intraepitheliale Dysplasie der kolorektalen Schleimhaut zum Karzinom. Die Dysplasie ist als eindeutige Neoplasie ohne invasives Wachstum definiert. Die Dysplasie ist histologisch durch zelluläre Atypie, abweichende Differenzierung und gestörte intraepitheliale Architektur gekennzeichnet. Ausgehend von dieser, von Vogelstein erstmals beschriebenen Adenom- Karzinom- Sequenz, ist davon auszugehen, dass im Laufe einiger Jahre aus fast allen kolorektalen Adenomen abhängig von verschiedenen Risikokonstellationen (s.u.) kolorektale Karzinome entstehen können. Die Zeitspanne vom Auftreten erster Veränderungen bis zur möglichen malignen Entartung beträgt in etwa 10 Jahre. Das Entartungspotential ist von mehreren Faktoren abhängig, es korreliert mit Typ, Größe und Grad der Dysplasie. Nach dem histologischen Aufbau werden Adenome unterteilt in tubuläre, tubulovillöse und villöse Formen, wobei letztere das höchste Entartungsrisiko aufweisen. Die Karzinomhäufigkeit bei tubulären Adenomen bei < 1cm liegt bei ca. 1%. Gleich große villöse Adenome zeigen bereits eine Entartungsfrequenz von 10%. Tubuläre Adenomen >2cm entarten in etwa 35% der Fälle, villöse Adenome von gleicher Größe bereits in über 50%. Als fortgeschrittene Adenome (advanced adenomas“) werden Adenome, die eine villöse, tubulovillöse Komponente oder hochgradige intraepitheliale Neoplasie aufweisen beziehungsweise tubulär wachsen und über 10 mm groß sind, zusammengefasst. Aufgrund ihrer histologischen Beschaffenheit und morphologischen Struktur wird davon ausgegangen, dass fortgeschrittene Adenome die Adenom Karzinom Sequenz“ besonders rasch und konsequent durchlaufen. Aus diesem Grund sollten alle Adenome des Kolorektums entfernt werden, die endoskopische Polypenabtragung stellt hierbei die Methode der Wahl dar. Die komplette Entfernung in einem Stück sollte angestrebt werden, da auf diese Weise eine präzise histologische Diagnostik möglich ist. Bezüglich hyperplastischer Polypen ist die wissenschaftliche Evidenz geringer. hyperplastische, insbesondere serratierte, Polypen des rechtsseitigen Colon sollten unabhängig von ihrer Größe entfernt werden; das gleiche gilt für größere hyperplastische Polypen im gesamten Colon. Bei den häufigen kleinenhyperplastischen Polypen/Polypenknospen des linksseitigen Kolons und Rektums scheint eine endoskopische Entfernung repräsentativer Läsionen ausreichend. Auch der familiären adenomatösen Polyposis coli (FAP) liegt die Adenom- Karzinom-Sequenz zugrunde und ist somit als obligate Präkanzerose zu bezeichnen. Die Erkrankung ist gekennzeichnet durch eine Mutation auf dem APC (Adenomatous Polyposis Coli Gen), welche autosomal dominant vererbt wird20. Bei der FAP treten mehr als hundert Adenome im Bereich des Kolorektums auf, meist beginnt das Wachstum nach der Pubertät, vorwiegend um das dreißigste Lebensjahr. Die Entwicklung zum Karzinom erfolgt meist um das das vierzigste Lebensjahr, wobei die Diagnose aufgrund der späten klinischen Symptomatik oft erst spät gestellt werden kann. Insgesamt ist etwa 1% aller kolorektalen Karzinome auf eine FAP zurückzuführen, Ein weiteres Modell der Entstehung kolorektaler Karzinome zeigt sich in der Gruppe der heriditären nicht- polypösen Kolonkarzinome (HNPCC), die etwa 5% aller kolorektalen Karzinome ausmacht. Hierbei werden 2 Typen unterschieden, Typ Lynch I zeigt eine Häufung kolorektaler Karzinome innerhalb von Familien ohne Assoziation mit extrakolischen Tumoren, Typ Lynch II ist durch eine familiäre Häufung des kolorektalen Karzinoms mit anderen Karzinomen (Endometrium, Ovar, Mamma, Pankreas, Haut, Larynx) gekennzeichnet. Im Rahmen dieser Syndrome sind der proximale Befall und eine Erkrankung im jungen Alter typisch. Ätiologisch wurde autosomal- dominante Abnormalität von Chromosom 2 mit einem Defekt im DNA- Replikationsreperaturmechanismus gefunden. Die durch Mutation inaktivierten missmatch-repair- (MMR-) Gene“ sind nicht mehr in der Lage, fehlerhaft replizierte DNA zu reparieren und führen so zu Akkumulation von Genmutationen, die die Zellproliferation direkt beeinflussen können. 70% der entstehenden Tumoren liegen proximal der linken Kolonflexur. Die Diagnose erfolgt durch Familienanamnese anhand der Amsterdam und Bethesda- Kriterien sowie molekulargenetischer Untersuchungen.Als weitere vererbbare kolorektale Tumordispositionserkrankungen seien der Vollständigkeit halber das Peutz- Jeghers- Syndrom sowie die familiäre juvenile Polyposis genannt. Patienten, welche an einer chronisch- entzündlichen Darmerkrankung leiden weisen ebenfalls eine erhöhte Inzidenz des kolorektalen Karzinoms auf. Der ständige Wechsel zwischen Epithelschädigung, Untergang und Regeneration wird als Ursache für die Karzinomentwicklung bei Patienten mit Colitis ulcerosa gesehen. Das Entartungsrisiko wird unter Berücksichtigung von Ausdehnung und Dauer der Erkrankung, Manifestationsalter, sowie im Rahmen endoskopischer Verlaufskontrollen verifizierter Dysplasie differenziert beurteilt. Die Literaturangaben bezüglich des Karzinomrisikos schwanken erheblich, als Richtwert ist ein etwa 10% höheres Karzinomrisiko nach einer Krankheitsdauer von etwa 20 Jahren zu rechnen. Liegt eine chronische Pankolitis vor, so erhöht sich das Risiko im gleichen Zeitraum auf 50%. Das Gesamtrisiko der malignen Entartung bei Morbus Crohn wird mit ca. 3% angegeben. Neben den endogenen Faktoren wie genetische Vorbelastung, Erkrankung an einer chronisch entzündliche Darmerkrankung sowie Patientenalter gibt es eine Reihe exogener Risikofaktoren (sogenannte life style factors“), die die Entstehung eines kolorektalen Karzinoms beeinflussen können. Bei diesem pathophysiologischen Modell des KRK ist Adenom- Karzinom- Sequenz genetisch determiniert und der Einfluss exogenabhängiger Risikofaktoren entscheidet über Protektion, Akzeleration und Geschwindigkeit der karzinomatösen Entartung. Da diese Aspekte in engem Zusammenhang mit derDarmkrebspävention stehen, werden sie im entsprechenden Kapitel behandelt.
Prävention
Präventivmaßnhamen sind beim kolorektalen Karzinom auf drei Ebenen möglich. Es wird unterschieden zwischen primärer, sekundärer und tertiärer Prävention:
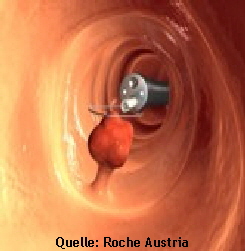
Primäre Prävention meint die Anwendung protektiver Maßnahmen um überhaupt die Entstehung von Adenomen und Karzinomen zu verhindern. Hierzu gehören Ernährungs- und Lebensstilfaktoren sowie Chemoprävention. (Ernährungsempfehlung: Zur Risikoreduktion eines kolorektalen Karzinoms sollte die Ballaststoffaufnahme erhöht werden. Rotes bzw. verarbeitetes Fleisch sollte nicht täglich verzehrt werden. Empfehlungsgrad: B,Evidenzstärke: 2a, starker Konsens. Obst und Gemüse sollten vermehrt gegessen werden. Eine Limitierung des Alkoholkonsums wird angeraten. Empfehlungsgrad: B, Evidenzstärke: 2b, starker Konsens.)Durch frühzeitige Bekämpfung der exogenen Risikofaktoren kann eine Inzidenzverminderung des KRK um 50% erwartet werden. Sekundäre Prävention umfasst die frühzeitige Erkennung von präkanzerösen Veränderungen (z.B. tubulovillöse Adenome) und von Frühkarzinomen und derenrechtzeitige komplette Entfernung. Die sekundäre Prävention ist somit die Domäne der interventionellen Endoskopie. Tertiäre Prävention schließlich beinhaltet die Nachsorge nach erfolgter Therapie eines kolorektalen Karzinoms und dient der Früherkennung von Lokalrezidiven oder Metastasen. (Quelle: ÖGGH)
|